このPTTHシリーズも(4)になったが、まだいくつか紹介したい研究裏話がある。今回はPTTHがホモダイマー構造をとっていることを発見したエピソードを紹介する。
(2)のPTTHのN末端アミノ酸配列分析の時に説明したが、どういう構造をしているか推測できれば、実験結果をその推測で説明できるかどうか確認することになる。しかし、実験結果から最初にモデルを作り上げるのは難しい。全ての実験データを頭にたたき込み、いろいろな条件を思い浮かべながら矛盾が出ないモデルを組み立てる必要がある。その後、そのモデルが正しいことを一つ一つ検証するのである。このモデルを組み立てる作業が研究者として最もエキサイティングで、能力(実力)を見せる場面である。
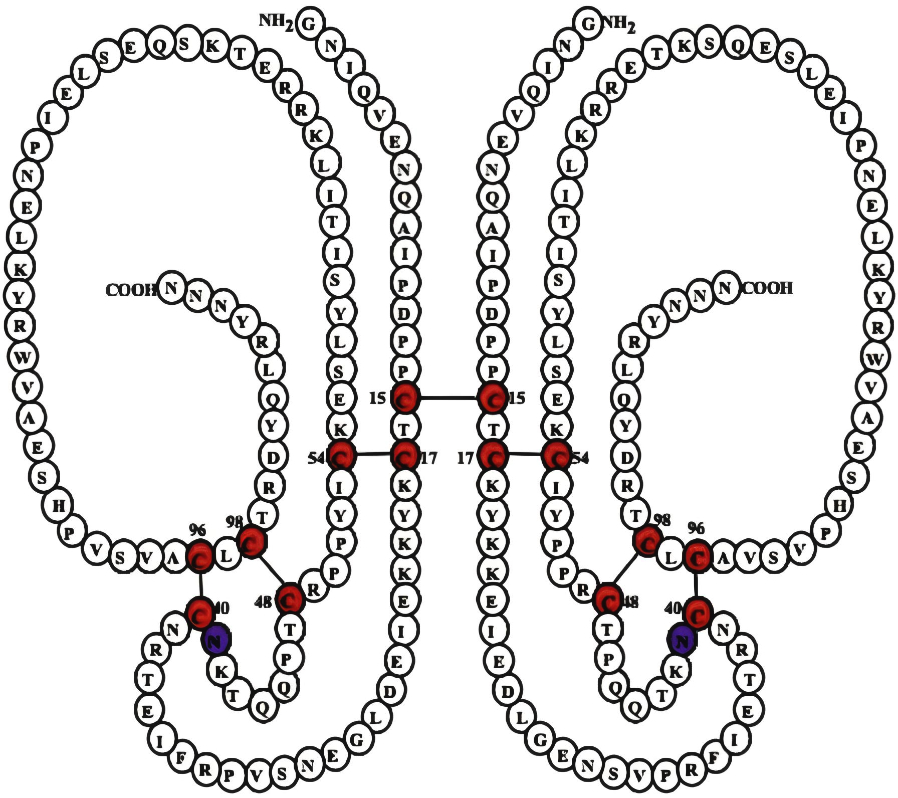
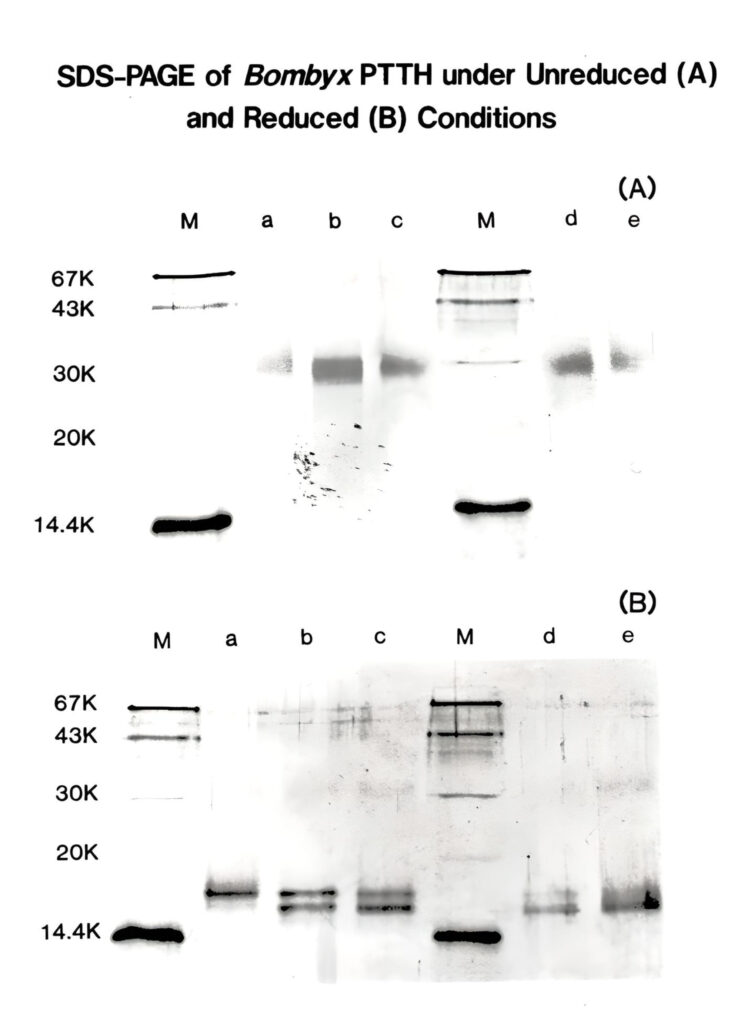
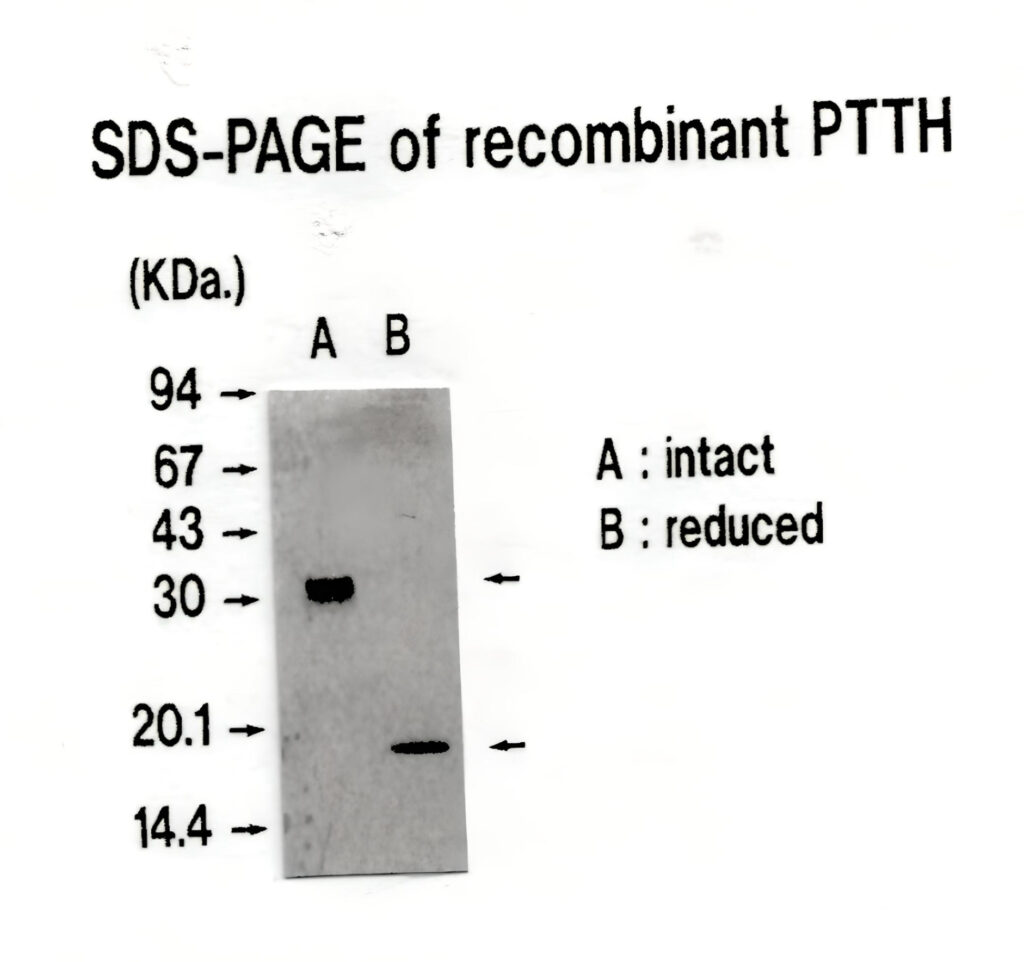
PTTHは(N末端やC末端の長さは異なるが)同じペプチド2本がジスルフィド結合で架橋したホモダイマー型ペプチドである(図1)。しかし、そのことが分かったのは構造決定(配列分析)がかなり進んだ博士課程3年生の秋であった。なぜだかPTTHは1本鎖ペプチドだと勝手に思い込んでいた。ある日、別の研究プロジェクトを行っていた卒論学生に、SDS-ゲル電気泳動(SDS-PAGE)で、精製PTTHを還元条件下と非還元条件下で分析してくれるように頼んだ。1本鎖なのでどちらもほぼ同じ分子量を示すことを確認するだけと考えていた。しかし、実験を行った学生から「還元条件下で、非還元条件下の分子量の約半分になってしまったのですが」と申し訳なさそうに言われ、いったい何が起きたのか一瞬理解できなかった。その後自分自身で、様々なロットの精製PTTHをSDS-PAGEで分析したり(図2)、還元アルキル化した後の配列分析などから、PTTHがジスルフィド結合で架橋したホモダイマー構造をもつと結論した。その後、大腸菌を使って合成したPTTHもホモダイマー構造をもつことを確認(図3)し、この大腸菌発現PTTHを用いてジスルフィド結合の架橋様式を決定した。この結果をもとにカイコPTTHの構造を示している(図1)。
PTTHがホモダイマー構造をとるとの重要な発見は、卒論学生に実験をお願いしたことで見つかった。確認しておく必要があることは、人の手を借りてでも実験することが大切である。ただし、最後は自分自身が実験して、きちんと証明する必要がある。ただ、いつでも手を借りられるように、人間関係を良好に保つことが研究者にも大切であることを自覚した。
ともかく、ペプチド(構造決定)屋からすると、PTTHはやっかいな分子であった。もし、ホモダイマー構造をとっていることが最初に分かっていたら、もっと華麗に構造決定できたと思う。結局、正しいモデルを、いかに早く構築(想像)できるかが研究者としての能力なのだろう。
-

前胸腺刺激ホルモン(PTTH)(6)
私が卒論研究として最初に従事した「カイコPTTHの生物検定法」を紹介したいと思… -



前胸腺刺激ホルモン(PTTH)(5)
今回は「PTTHが昆虫種間で交差活性を示さない」ことから起きた研究裏話を紹介し… -



前胸腺刺激ホルモン(PTTH)(3)
微量物質を精製して構造を決めるためには、大量の材料から精製することが必要で… -



前胸腺刺激ホルモン(PTTH)(2)
研究の流れに沿って裏話やエピソードを紹介することもできるが、ここでは、私が… -



前胸腺刺激ホルモン(prothoracocotropic hormone、PTTH)(1)
この前胸腺刺激ホルモン (PTTH)研究は、私のライフワークと言える。1980年の卒…