研究成果
生物は、ホルモンなど固有の情報分子を利用した様々な調節・制御系を持ち、細胞の分化・増殖、生理状態をコントロールし、個体として、また種として統一が取れた生命の維持を行っています。
これらの調節・制御系に関わる生体情報分子であるペプチドホルモン(神経ペプチド)やステロイドホルモンなどに注目して、それらの化学構造や生合成経路を明らかにするとともに、細胞膜や細胞内に存在する受容体分子によって認識される過程、それによって引き起こされる細胞や個体の機能変化について研究を進めました。
1922年、S. Kopecは昆虫の脳がホルモンを分泌して変態を制御していることを発表しましたが、当時の常識では脳が内分泌器官であるとは信じられず、しばらく顧みられることはありませんでした。1950年代になって、V. B. WigglesworthやC. Williamsらによって現在クラシカルスキームと呼ばれている昆虫の脱皮・変態の制御機構が明らかにされました。すなわち、脳から分泌される前胸腺刺激ホルモン(PTTH)が前胸腺に作用して脱皮ホルモン(ステロイドホルモンであるエクジソン)の合成・分泌を促し、その作用で新しい表皮が形成されます。この時にアラタ体から幼若ホルモンが分泌されていると幼虫脱皮が、幼若ホルモンの分泌が抑えられていると幼虫から蛹へ、さらに成虫へと変態が起きます。エクジソンと幼若ホルモンは1960年代に欧米の研究者によって単離・構造決定されましたが、PTTHは1960年代にペプチド性の物質(神経ペプチド)であることが分かり、世界中の多くの昆虫学者が精製を試みましたが、1980年代まで誰も単離に成功しませんでした。
片岡の最大の業績は、数百万頭のカイコ蛾頭部からわずか数十マイクログラムのPTTHを単離してアミノ酸配列を明らかにしたことです。精製したペプチドからアミノ酸配列を解明できたのは、数多くの昆虫のうちカイコPTTHだけです。さらに、アミノ酸配列だけではなく、PTTHがジスルフィド結合を介したホモダイマー構造をしていることや、41残基目に付加している糖鎖構造も明らかにしました。また、共同研究者とともに、様々な昆虫のPTTH遺伝子のクローニング、大腸菌を用いた活性型PTTHの大量発現やELISA法による血液中濃度の微量定量系の確立などを行って、PTTHによる脱皮・変態調節機構解明の礎を築きました。
さらに、神経ペプチドによるエクジソン生合成調節機構の全容解明を目指してカイコ前胸腺に作用する神経ペプチド類の精製・構造解析を行いました。1999年に前胸腺抑制ペプチド(PTSP)を単離したのを皮切りに、2005年にエクジソン合成を抑制する神経ペプチド、ミオサプレッシン(MS)を単離・構造決定しました。また、MSに関連するペプチド類を精製し、それらがMS遺伝子とは別の遺伝子にコードされたFMRFアミド関連ペプチド(FaRP)であり、同じく前胸腺抑制活性があることを明らかにしました。加えて、FaRPは血液を介さず、胸部神経節で作られた後、前胸腺へ延びる神経軸索で運ばれるという新規経路で作用することも示しました。PTSP、MS、FaRPのような前胸腺のエクジソン合成を抑制する神経ペプチドが複数存在する理由は、栄養を十分取って成長するまで、脱皮・変態が進まないように、二重三重に抑制をかけるためだと考えられます。また、温帯に生息する多くの鱗翅目昆虫は蛹期に発育を停止する蛹休眠が観察されますが、MSがこの蛹休眠を誘導することも共同研究者とともに解明しました。
片岡は1986年から2年間米国に留学し、羽化行動を誘導する羽化ホルモン(EH)、羽化後に利尿を誘起する利尿ホルモン(DH)、幼若ホルモンの生合成を調節するアラタ体刺激ホルモン(アラトトロピン、AT)とアラタ体抑制ホルモン(アラトスタチン、AS)の神経ペプチド類をタバコスズメガ頭部から精製して、その構造を世界に先駆けて明らかにしました。いずれの神経ペプチドもそれまでに多くの研究者によって精製が試みられましたが、成功していませんでした。
さらに、神経ペプチド類の作用機序にも興味をもち、神経ペプチド受容体の多くがGPCR(Gタンパク質共役受容体)であることに着目して、カイコゲノム上に存在するGPCRの網羅的解析を行いました。その結果、カイコゲノム配列から47種類のGPCRを同定しました。また、発育ステージの異なる12種類の組織を用いて定量PCR法によりGPCR遺伝子の時空間的な発現量の変化を解析した結果、組織ごとに発現しているGPCRの種類が異なることや発育時期によって発現量が大きく変化することを明らかにしました。その過程で、前胸腺に発現しているGPCRのリガンド同定も進め、前胸腺活性化因子として、FXPRL-アミド類(FXPRLa)や、色素胞拡散因子(PDF)の神経ペプチドを新たに同定しました。
一方、液体クロマトグラフィー−タンデム質量分析(LC-MS/MS)を用いたエクジソン生合成関連ステロイド類の微量定量法を確立しました。この手法を用いてエクジソン生合成酵素の基質を解明するとともに、発育に伴う組織中のステロイド類の変動も解析しました。この方法は、従来の放射性免疫法(RIA法)では測定できなかったコレステロールや生合成中間体も高感度で、しかも個別のステロイドを区別して10分以内に一斉定量できる画期的な定量法です。また、カイコ、ヨトウガなどの昆虫だけでなく、ダニのエクジソン生合成酵素類を世界に先駆けて明らかにしました。さらに、カイコ生合成酵素類の各遺伝子発現が神経ペプチド類によって促進または抑制されることも明らかにしました。
主な研究論文
(1) H. Kataoka, H. Nagasawa, A. Isogai, S. Tamura, A. Mizoguchi, Y. Fujiwara, C. Suzuki, H. Ishizaki and A. Suzuki. (1987) Isolation and partial characterization of prothoracicotropic hormone of the silkworm, Bombyx mori. Agric. Biol. Chem., 51, 1067-1076.
(2) H. Kataoka, A. Toschi, J. P. Li, R. L. Carney, D. A. Schooley and S. J. Kramer. (1989) Identification of an allatotropin from adult Manduca sexta. Science, 243, 1481-1483.
(3) H. Kataoka, H. Nagasawa, A. Isogai, H. Ishizaki and A. Suzuki. (1991) Prothoracicotropic hormone of the silkworm, Bombyx mori: amino acid sequence and dimeric structure. Agric Biol. Chem., 55, 73-86.
(4) Y.-J. Hua, Y. Tanaka, K. Nakamura, M. Sakakibara and H. Kataoka. (1999) Identification of a prothoracicostatic peptide (PTSP) from the larval brain of the silkworm, Bombyx mori. J. Biol. Chem., 274, 31169-31173.
(5) N. Yamanaka, Yue-Jin Hua, A. Mizoguchi, K. Watanabe, R. Niwa. Y. Tanaka and H. Kataoka. (2005) Identification of a novel prothoracicostatic hormone and its receptor in the silkworm, Bombyx mori. J. Biol. Chem., 280, 14684-14690.
(6) N. Yamanaka, D. Zitnan, Y-J. Kim, M. E. Adams, Y-J. Hua, Y. Suzuki, M. Suzuki, A. Suzuki, H. Satake, A. Mizoguchi, K. Asaoka, Y. Tanaka and H. Kataoka. (2006) Regulation of insect steroid hormone biosynthesis by innervating peptidergic neurons. Proc. Natl. Acd. Sci. USA., 103, 8622-8627.
(7) N. Yamanaka, N. Honda, N. Osato, R. Niwa, A. Mizoguchi and H. Kataoka. (2007) Differential regulation of Ecdysteroidogenic P450 gene expression in the silkworm, Bombyx mori. Biosci. Biothech. Biochem., 71, 2808-281
(8) F. Igarashi, J. Hikiba, M. H. Ogihara, T. Nakaoka, M. Suzuki and H. Kataoka. (2011) A highly specific and sensitive quantification analysis of the sterols in silkworm larvae by HPLC/APCI-MS/MS. Anal. Biochem., 419, 123-132.
(9) J. Hikiba, M. H. Ogihara, M. Iga, K. Saito, Y. Fujimoto, M. Suzuki, and H. Kataoka. (2013) Simultaneous quantification of individual intermediate steroids in silkworm ecdysone biosynthesis by liquid chromatography-tandem mass spectrometry with multiple reaction monitoring. J. Chromatography B, 915-916, 52-56.
(10) S. Nagata, J. Kobayashi, H. Kataoka and A. Suzuki. (2014) Structural determination of an N-glycan moiety attached to the prothoracicotropic hormone from the silkmoth Bombyx mori. Biosci. Biothech. Biochem., 78, 1381-1383.
(11) M. H. Ogiahra, D. Taylor and Hiroshi Kataoka. (2019) Steroid hormone in Acari, its function and synthesis. Applied Entomology and Zoology, 54, 323-338.
主要な研究テーマ
昆虫の脱皮・変態は、ホルモンで厳密に調節されています。それは、 前胸腺 という器官で合成されるステロイドホルモンであるエクジソンによって制御されているためです。エクジソンは、脊椎動物のエストロゲン受容体に似た核内受容体を介して様々な遺伝子の転写を制御しています。その結果、細胞増殖・予定細胞死・神経系の成熟・クチクラ形成などが誘導され、最終的に脱皮・変態が引き起こされます。しかし、その肝心のエクジソンの生合成酵素や生合成経路は、未同定の部分(Black Box)が存在します。これまで、私たちのグループでは、いくつかのエクジソンの生合成酵素を同定してきました。
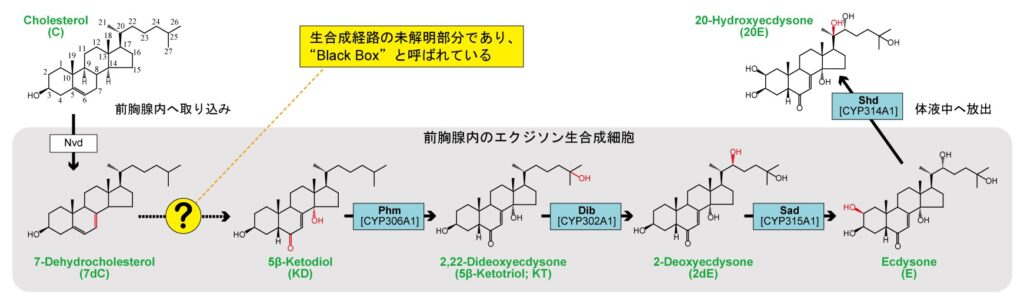
生合成経路解明に向けた分析手法の開発(クリックで詳細を表示)
昆虫は、ステロイド骨格を形成する生合成経路を持たないため、食餌から取り込んだコレステロールや植物ステロール類を利用して 前胸腺 でステロイドホルモン(エクジソン)を生合成しています。そこで、生合成経路全貌解明に向けて、原料となるステロール類や生合成中間体エクジステロイド類を一斉に微量定量できる手法を開発しました。
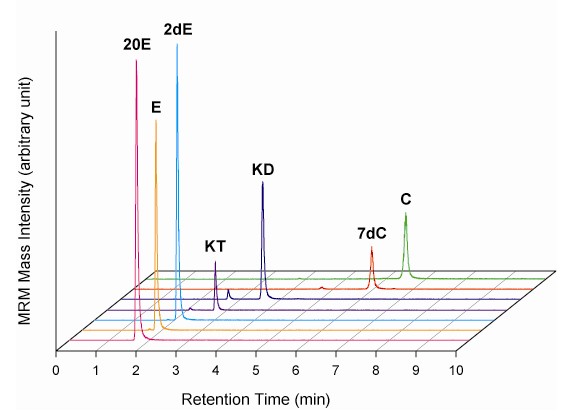
液体クロマトグラフィーで分離した化合物をタンデム型質量分析計で検出する、いわゆるLC-MS/MSと呼ばれる分析システムを導入し、MS/MS検出にはMultiple Reaction Monitoring(MRM)という方法を採用しました。MRMでは、親イオンの質量数に加えてフラグメントイオンの質量数でも検出フィルターをかけるため、化合物検出の選択性や感度が向上します。例えば、右の図は、上述のエクジソン生合成経路に現れる7つのステロイドをそれぞれ1.0 ng含む混合溶液を分析したときの各MRMチャンネルのクロマトグラムを示しています。1回の試料注入で7つのステロイドすべてを分離して検出できています。また、この分析法の特長として広い測定レンジを持っていることがあげられ、ステロイドの種類にも依りますが、おおよそngレベルからμgレベルまでのステロイド類を同時に定量することができます。
まず、私たちは、この手法をカイコ幼虫における食餌由来のステロール類の体内分布の解析に応用しました[1]。カイコの体内には様々なステロール類が検出されますが、器官によってその分布は異なり、例えば、コレステロールは脳で比較的含量が高いのに対して、エクジソン生合成中間体である7-デヒドロコレステロールは 前胸腺 にしか検出されません。
また、私たちは、この手法を用いてカイコ幼虫の 前胸腺 および体液中のエクジソン生合成中間体の分析を行いました[2]。体液中にエクジソンが放出されるエクジソン生合成が盛んな時期であっても、 前胸腺 内には5β-ケトジオールや5β-ケトトリオールは検出されず、生合成経路の中でもそれらのステロイドの変換反応は速い反応であると考えられます。
現在、この手法は、生合成経路全貌解明に向けて、 前胸腺 へのステロール類の取り込みの解析、 前胸腺 における未知の生合成中間体ステロイドの探索、生合成酵素のステロイド変換活性の測定など、幅広い実験に活用されています。
[1] Igarashi et al.: Anal. Biochem., 419, 123–132 (2011). 
[2] Hikiba et al.: J. Chromatogr. B, 915–916, 52–56 (2013). 
哺乳類のステロイドホルモンの合成・分泌は、視床下部-下垂体系を中心とするフィードバック機構によって制御されています。昆虫においても、エクジソンの生合成は、体内外の環境情報をもとに脳神経系で合成される複数のペプチドホルモン(神経ペプチド)によってさらに調節されています。私たちは、 前胸腺刺激ホルモン 、前胸腺抑制ペプチド、ミオサプレッシン、FMRF-アミド関連ペプチド、PDFなどの神経ペプチド群によって、エクジソン生合成が巧妙に調節されていることを明らかにしてきました。
昆虫は冬のような生育に不適な時期を乗り切るために「休眠」というシステムを獲得しました。冬に見られる休眠は、低温による受動的な発育停止ではなく、日長変化などの環境要因から冬の到来を予期して、あらかじめ成長を停止させるようなプログラムを発動させる能動的な適応戦略です。この休眠も脱皮・変態と同じくエクジソンによってコントロールされています。さらに、休眠も神経ペプチド群による調節を受けています。また、卵の休眠はエクジソンがリン酸化されて不活性化することで誘導されることが知られています。しかしながら、環境情報がどのように認識され、どのようにエクジソンの分泌抑制や不活性化につながるのか、についてはよくわかっていません。また、休眠から覚醒する際に必要なシグナルも同様に未解明です。昆虫が環境情報をどのように感知し、どのように内分泌シグナルに反映させて発生のタイミングを制御しているのかといった問題に取り組みました。
参考文献
doi: 10.1016/j.ibmb.2020.103491
doi: 10.1111/imb.12291
doi: 10.1038/srep41651
doi: 10.1371/journal.pone.0146619
doi: 10.1371/journal.pone.0060824




